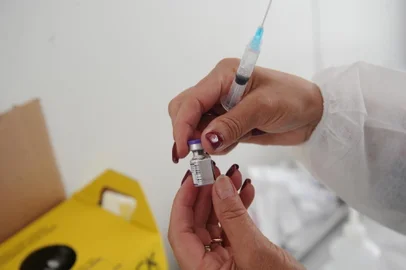
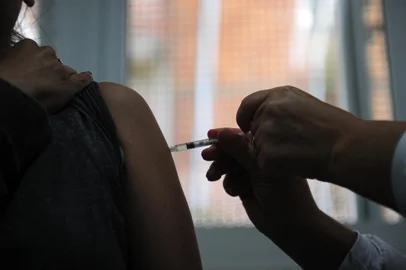
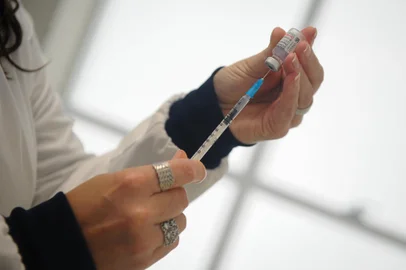
Menos propensos a desenvolverem casos graves de covid-19 na comparação com idosos e pessoas com doenças prévias, as crianças e os adolescentes já estão no horizonte das farmacêuticas produtoras de vacinas contra o coronavírus. Ainda que a expectativa seja de que esses imunizantes não vão chegar tão cedo a esse público, os laboratórios começaram a ampliar seus estudos para abranger indivíduos com menos de 18 anos. Das companhias que têm uso emergencial aprovado no Brasil, Sinovac, Oxford/ AstraZeneca e Janssen já iniciaram os estudos em crianças e adolescentes. A Pfizer, que tem registro definitivo no país, também avança nos testes (leia abaixo).
O fato desse grupo etário ter ficado de fora das pesquisas iniciais das vacinas contra a covid-19 se deve, principalmente, a dois motivos, explica o médico Marcelo Comerlato Scotta, infectologista pediátrico do Hospital Moinhos de Vento (HMV): crianças e adolescentes têm quadros menos graves da doença e questões regulatórias do país envolvendo estudos com essa faixa etária.
— Eles podem fazer quadros graves, apesar de isso ser muito menos frequente do que em adultos. E tem o aspecto regulatório no Brasil. Estudos clínicos em pediatria são feitos depois da testagem em adultos — justifica Scotta.
Enquanto não saírem os resultados dos estudos clínicos e aprovação para uso, a aplicação de vacinas contra a covid-19 nessa faixa etária não é permitida, destaca o médico do HMV.
Pesquisas em andamento
O movimento de incluir crianças e adolescentes nas pesquisas é uma extensão natural do licenciamento, acrescenta Renato Kfouri, diretor da Sociedade Brasileira de Imunizações (SBIm). Segundo ele, a tendência desses trabalhos é de que eles sejam mais rápidos, pois não precisam incluir uma quantidade tão grande de voluntários. Nesses casos, são feitos os chamados estudos ponte: se a resposta imune for semelhante à do adulto, acaba-se inferindo a eficácia nesse público mais jovem.
Porém, da comprovação de segurança e eficácia até chegar aos braços do público mais jovem deve-se esperar um longo caminho pela frente. A produção desses imunizantes ainda é um gargalo importante, e, portanto, a prioridade dos programas de imunização neste momento é reduzir as complicações e mortes, argumenta Kfouri.
— Daqui a pouco serão liberadas para crianças acima de 10 anos e isso não mudará nada. Neste momento, o objetivo é diminuir as hospitalizações e mortes, e não a circulação. Por isso, a maioria dos programas de vacinação são voltados para públicos mais vulneráveis. Quando pensar mais para frente, em mudar o objetivo da vacinação para diminuir a transmissão e eliminar o vírus, aí teremos que incluir crianças e adolescentes. Nesse momento, o objetivo deixará de ser prevenção de formas graves — diz o diretor da SBIm.
Contudo, completa o médico da SBIm, dentro do grupo das crianças e adolescentes, existe um subgrupo de risco, no qual estão incluídos pacientes em diálise, oncológicos, diabéticos e transplantados, entre outros vulneráveis. Para esses, a imunização seria mais importante, avalia.
— Esse é um dos objetivos desses estudos — fala.
O Ministério da Saúde informou, por meio de sua assessoria de imprensa, que acompanha e financia estudos de análise de efetividade e segurança das vacinas contra a covid-19 em pessoas com menos de 18 anos. A inclusão desses produtos no Programa Nacional de Imunizações (PNI), no entanto, depende da conclusão dessas pesquisas e da avaliação conjunta da Câmara Técnica e demais envolvidos.
Como estão os testes*
- Oxford/ AstraZeneca: os estudos começaram em fevereiro, no entanto, foram pausados no começo de abril para aguardar mais informações sobre os raros problemas de coagulação em adultos que receberam as doses. O estudo testa a vacina na faixa de seis a 17 anos.
- Sinovac: testes em crianças e adolescentes, de três a 17 anos, mostraram bons resultados de segurança e eficácia nas fases 1 e 2, informou a companhia, em março.
- Pfizer/ BioNTech: no dia 31 de março, a companhia anunciou que a fase 3 dos estudos com adolescentes de 12 a 15 anos demonstrou eficácia de 100% e respostas robustas de anticorpos. Em março, a companhia anunciou os testes na faixa dos seis meses até os 11 anos. Até o momento, a vacina tem aprovação para uso em pessoas a partir dos 16 anos
- Janssen: começou, em 2 de abril, a testar a vacina em adolescentes na fase 2 do estudo clínico. A pesquisa inclui jovens de 12 a 17 anos.
*apenas imunizantes autorizados no Brasil