O Instituto de Tecnologia em Imunobiológicos da Fundação Oswaldo Cruz (Bio-Manguinhos/Fiocruz) pediu o registro de dois kits de diagnóstico molecular do vírus da varíola dos macacos, também conhecido como monkeypox, junto à Agência Nacional de Vigilância Sanitária (Anvisa).
O vírus é considerado uma emergência de saúde pública internacional pela Organização Mundial da Saúde (OMS), e a Anvisa já recebeu um total de seis pedidos de registro de kits para o diagnóstico da doença.
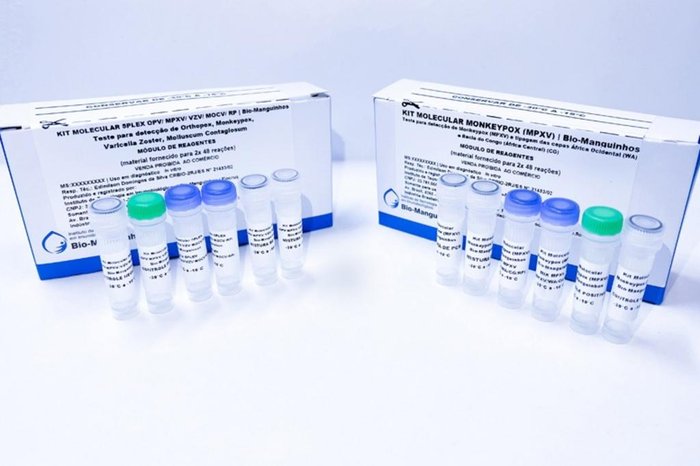
Um dos kits produzidos pela Fiocruz, chamado kit molecular monkeypox (MPXV), é capaz de fazer a identificação das duas cepas do vírus que circulam de forma endêmica no continente africano. Apenas uma delas, a da África Ocidental, é a responsável pelo surto em outros continentes.
Esse teste é do tipo PCR e consegue identificar o DNA desses dois tipos de vírus em amostras retiradas das erupções cutâneas presentes no indivíduo com suspeita de infecção.
O segundo kit que teve seu registro solicitado no Brasil é para o diagnóstico diferencial, em que outras possibilidades de diagnóstico por vírus relacionados são descartadas.
Com os testes, será possível adotar dois protocolos: no protocolo 1, com o teste MPXV, é feita a detecção e tipagem do monkeypox. Em caso de teste negativo, o protocolo 2 aumenta a possibilidade de definição do diagnóstico com a utilização do teste diferencial. Segundo a Fiocruz, isso é importante para a vigilância epidemiológica no Sistema Único de Saúde (SUS).
Além de ter desenvolvido e solicitado o registro dos testes, o Bio-Manguinhos já produziu o suficiente para realizar 12 mil testes em casos suspeitos e afirma ter condições de escalonar a produção desses kits sem prejudicar o fornecimento de outros produtos de seu portfólio.
Para a presidente da Fiocruz, Nísia Trindade Lima, uma cadeia de suprimentos mais efetiva e um arranjo produtivo local fortalecido contribuem para a autonomia nacional em relação a insumos indispensáveis ao enfrentamento de problemas de saúde pública.
Outros pedidos
Além dos dois pedidos feitos pela Fiocruz, a Anvisa também analisa outros quatro exames. Os dois primeiros pedidos protocolados são Viasure Monkeypox Virus Real Time PCR Detection Kit, fabricado na Espanha pela empresa CerTest Biotec, e Monkeypox Virus Nucleic Acid Detection Kit, fabricado na China pela empresa Shanghai BioGerm Medical Technology Co., Ltd. Ambos são ensaios moleculares, passaram pela avaliação do corpo técnico e aguardam complementação de informações por parte das empresas solicitantes para continuidade da análise.
O terceiro produto, que teve o pedido de registro submetido na segunda-feira (8), também é um ensaio molecular e corresponde ao Standard M10 MPX/OPX, que tem como fabricante legal a empresa nacional Eco Diagnóstica, mas que tem parte da sua produção ocorrendo em outro país. A análise técnica da documentação está em curso.
Na quarta-feira (10), um pedido de teste rápido chegou na agência reguladora, o Monkeypox Virus Antigen Rapid Test, fabricado pela empresa chinesa Bioscience (Tianjin) Diagnostic.
Em seu site, a Anvisa disse que "vem priorizando a avaliação de todos os pedidos de registro de produtos para diagnóstico in vitro que possam ser utilizados como recurso para o enfrentamento da Monkeypox".