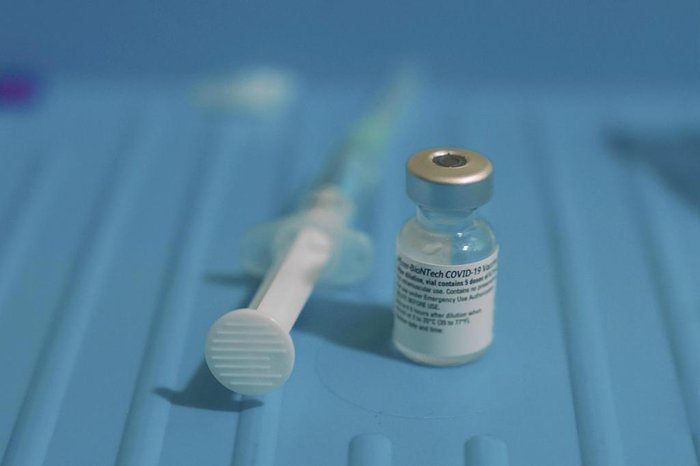
O comitê de especialistas da agência reguladora de medicamentos dos Estados Unidos (FDA) votou nesta quinta-feira (10) a favor da recomendação ao uso da vacina Pfizer/BioNTech contra covid-19 no país. A votação não é vinculativa e o sinal verde para a comercialização ainda não foi dado, o que caberá ao FDA determinar nos próximos dias. A decisão, porém, esclarece dúvidas sobre o tratamento.
A vacina poderia começar a ser administrada nos Estados Unidos no início da próxima semana em hospitais e casas de repouso, de acordo com a secretaria de saúde dos EUA. Após duas doses, a vacina foi considerada segura, sem efeitos colaterais graves, e 95% eficaz na prevenção da covid-19, doença causada pelo coronavírus.
A primeira dose parece começar a proteger o paciente após dez dias, mas menos do que com a dose complementar, três semanas depois.
— As respostas imunes provocadas pelo RNAm (RNA mensageiro) são semelhantes às da infecção natural. Mas, é claro, a vacina de RNAm não é infecciosa e não pode causar doenças — disse Kathrin Jansen, diretora de vacinas da Pfizer, durante uma sessão de perguntas e respostas com o comitê.
Os especialistas do comitê debateram extensivamente o risco de alergia da vacina, após o surgimento de dois casos de reações graves no Reino Unido. Nos Estados Unidos, um alerta acompanhará a vacina não será recomendada para pessoas com alergia a algum de seus ingredientes.






