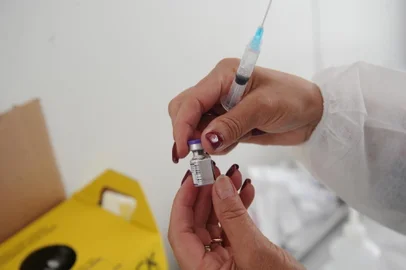
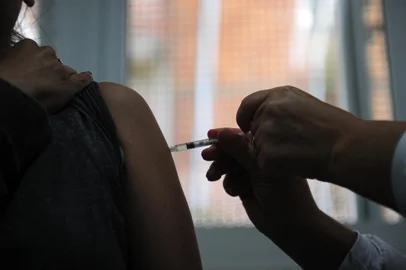
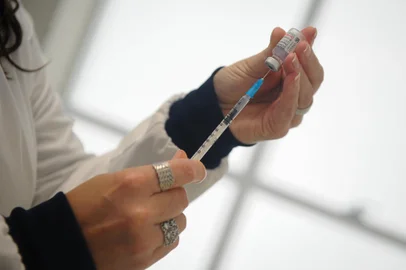
Um ofício foi encaminhado nesta sexta-feira (13) pela Agência Nacional de Vigilância Sanitária (Anvisa) ao laboratório farmacêutico Pfizer solicitando informações sobre estudos relacionados à aplicação de uma terceira dose do imunizante contra a covid-19, vacina chamada de Comirnaty.
O intenção do órgão brasileiro é descobrir o que motivou a agência reguladora norte-americana (Food and Drug Administration - FDA) publicar memorando que orienta aplicação de uma dose extra em caso de pacientes transplantados ou imunocomprometidos, que possuem mecanismos de defesa contra infecção já comprometidos em função de alguma comorbidade.
A Anvisa pediu que o laboratíorio divulgue informações sobre a participação da Pfizer na condução dos estudos feitos em território americano e os resultados parciais já obtidos. Além disso, a agência Brasileira solicitou reunião com a farmacêutica para discutir o uso de uma terceira dose ou aplicação de reforço do imunizante.
No Brasil, a Pfizer já recebeu autorização da Anvisa no dia 18 de junho para conduzir um estudo clínico de avaliação da eficácia e segurança da aplicação de uma terceira dose de sua vacina. A condução e andamento dos estudos é de responsabilidade dos laboratórios patrocinadores da pesquisa. Além do programa da Pfizer/BioNTech, outros dois pedidos de estudo sobre doses extras estão em andamento no Brasil - ambos envolvem o laboratório Astrazeneca.